在现代科技和日常生活中,蓄电池作为一种常见的能量存储装置,对我们的影响无处不在。关于蓄电池放电过程,有一个经常被讨论的问题:“蓄电池放电是物理变化吗?”这个问题涉及到化学反应和能量转换的原理。本文将从科学的角度深入探讨蓄电池放电的原理,并解答这个备受关注的问题。
蓄电池放电的科学原理
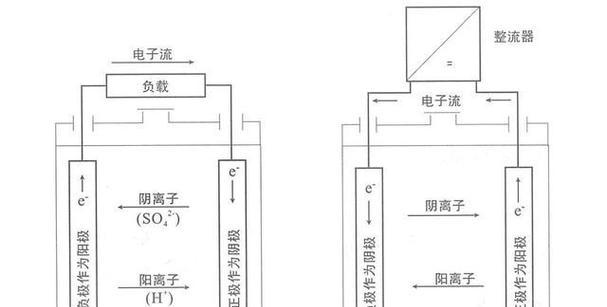
蓄电池放电是一个复杂的化学和物理过程。它涉及到电解液中的离子运动、电极材料的化学反应以及电能与化学能之间的转换。通常,蓄电池主要通过电极反应来释放储存的化学能,转化为电能输出。
以铅酸蓄电池为例,放电时,负极的铅(Pb)与硫酸(H2SO4)发生化学反应,生成硫酸铅(PbSO4)和电子,而正极的二氧化铅(PbO2)与硫酸和电子反应,同样生成硫酸铅(PbSO4)。整个反应过程可以用以下化学方程式表示:
```
负极:Pb+H2SO4→PbSO4+2H++2e?
正极:PbO2+H2SO4+2e?→PbSO4+2H2O
```
蓄电池放电是否为物理变化?
现在我们来回答这个问题。我们需要明白什么是物理变化,什么是化学变化。物理变化指的是物质形态或物理性质的改变,但不改变物质的化学成分;而化学变化则指的是物质的化学成分发生改变的过程。
从上面的描述中可以看出,蓄电池放电过程中,电极材料的化学成分确实发生了改变。负极的铅变成了硫酸铅,正极的二氧化铅也变成了硫酸铅。根据化学变化的定义,蓄电池放电属于化学变化。
放电过程中的物理变化
虽然蓄电池放电主要是化学变化,但这并不意味着其中没有物理变化。放电过程中的确存在一些物理变化,比如电解液浓度的变化、温度的升高,以及电池内部微观结构的改变。这些变化在电池使用过程中起到辅助作用,但主要变化还是化学性质的改变。

蓄电池放电原理的深度探究
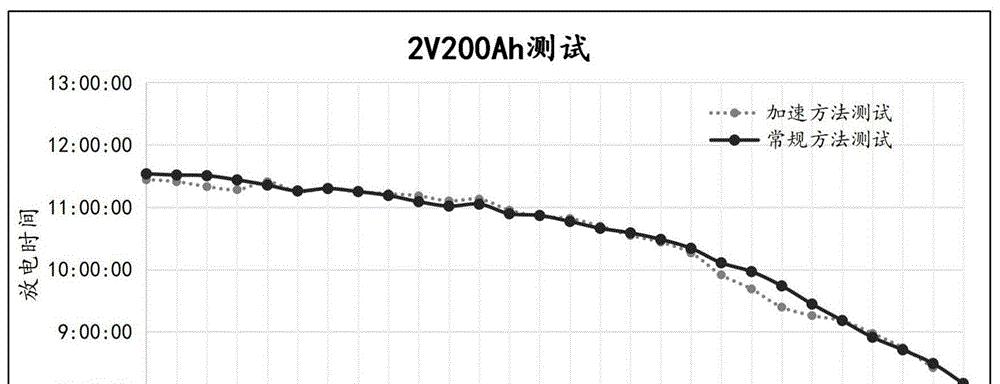
深入理解蓄电池放电原理不仅有助于我们回答前面的问题,还有助于我们更好地使用和维护蓄电池。蓄电池在放电过程中,其电压会随着放电深度的增加而逐渐降低。当电压下降到某一临界值时,就必须停止放电,以防止电池过度放电而损坏。了解这些原理,可以帮助用户判断何时应该充电,以及如何合理使用电池,延长其使用寿命。
结论
综上所述,蓄电池放电是一个主要的化学变化过程,它涉及电极材料的化学成分的转变。当然,放电过程中也伴随着一些物理变化,但这些变化不是主要的。了解蓄电池放电的化学与物理原理,不仅能够让我们更加科学地使用和维护蓄电池,还能帮助我们理解电池技术的发展方向,对相关科技领域的进步有更深刻的认识。